
近日,深圳理工大学药学院特任副教授邹帆团队联合广州医科大学附属妇女儿童医疗中心、中山大学附属第三医院、广州医科大学附属第二医院及湖北省第三人民医院等单位,在Advanced Science期刊发表最新研究成果,提出了“免疫桥接”治疗范式,通过唤醒人体自身的抗病毒体液免疫反应,让其“调转枪头”精准攻击癌细胞。这一创新方式,相当于给人体自身的抗病毒免疫力重新赋能,让其能特异性瞄准并杀死癌细胞,为肿瘤治疗开辟了全新的技术路径和临床思路。
该研究提出了一种可将疫苗诱导的抗体重定向至肿瘤免疫检查点的新型策略,具有显著的机制原创性与临床转化价值,入选Wiley Research Headlines全球亮点研究推荐。

论文上线截图

聚焦临床痛点
瞄准核心科学问题
目前肿瘤免疫治疗面临的核心瓶颈,主要是肿瘤抗原的异质性丢失与免疫原性不足。通俗讲就是肿瘤细胞很会“伪装”,要么不断改变自身特征,让免疫系统认不出;要么自身的辨识度太低,免疫系统注意不到它。尽管PD-L1是实体瘤免疫治疗的经典靶点,但现有抗体药物单药响应率有限,且难以应对抗原下调导致的耐药问题。
与此同时,人体在疫苗接种(如带状疱疹、麻疹、乙肝疫苗)或自然感染病毒后,会产生抗病毒免疫力——包括高浓度IgG抗体和病毒特异性记忆T细胞,可它们却长期处于“休眠”状态,没能被抗肿瘤免疫有效调动起来对抗肿瘤。

核心创新:
PBAP-gE搭建“免疫桥梁”
为了解决这个问题,研究团队设计了一种名为PBAP-gE(PD-L1-Binding Antigen Presenter)的模块化双功能蛋白复合物。该分子以可溶性PD-1(sPD-1)为“锚”,特异性结合肿瘤细胞表面的PD-L1;同时以带状疱疹病毒糖蛋白E(gE)为“饵”,展示于肿瘤细胞表面。
当人体因接种LZ901重组带状疱疹疫苗(绿竹生物)而存在预存抗gE抗体时,这些抗体就会成为关键的“分子桥梁”:一端结合肿瘤表面的PBAP-gE,另一端通过自身的Fc段,连接到NK细胞表面的FcγRIIIa(CD16)受体,进而强烈激活抗体依赖性细胞介导的细胞毒性(ADCC)效应——简单说,就是让NK细胞快速认清肿瘤细胞,精准发起攻击,杀死肿瘤细胞。
这一策略巧妙地将“抗病毒免疫记忆”转化为“抗肿瘤免疫效应”,无需等待免疫系统重新学习或识别肿瘤,即可实现“即插即用”的快速应答,提升了治疗效率。
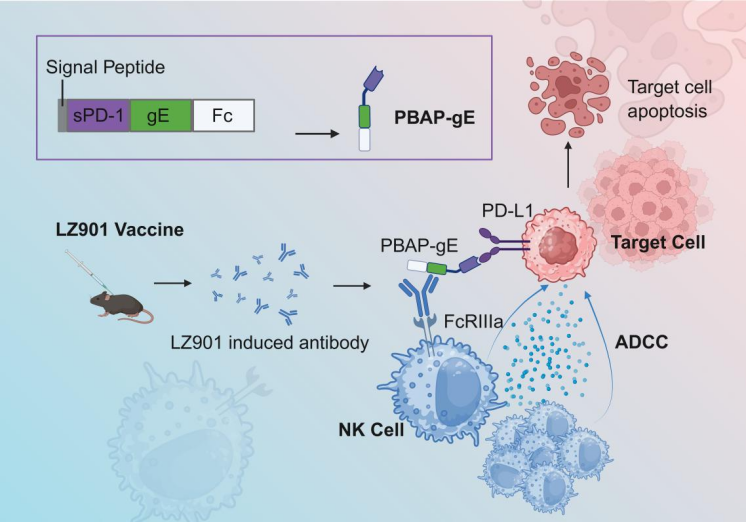
PBAP-gE联合LZ901疫苗诱导抗体协同NK细胞发挥抗肿瘤活性示意图

精准递送:
CAR-T介导“活药”靶向给药
为避免PBAP在血液循环中被预存抗体中和,研究团队进一步开发了第四代CAR-T递送系统,相当于给PBAP装上了精准导航与智能开关。将PBAP基因置于诱导型启动子控制下,让CAR-T细胞仅在识别肿瘤抗原并被激活后才分泌PBAP蛋白。这种“活体药物”(Living Drug)递送策略实现了时空特异性的蛋白释放:既保证了PBAP在肿瘤部位的局部高浓度,又显著降低了系统毒性,减少对正常细胞的损伤。同时,CAR-T细胞能在体内长期存活,相当于为身体建立了免疫记忆,实现了对肿瘤的持久巡防。
实验证实,该递送系统的抗肿瘤效果可媲美瘤内直接注射,展现了优异的临床转化潜力。
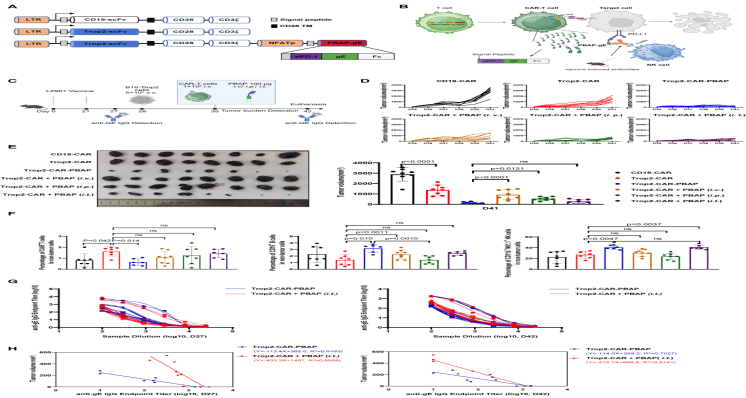
CAR-T细胞递送系统实现媲美瘤内注射的PBAP-gE精准释放与免疫记忆诱导

模块化拓展
打破抗原限制
该研究的另一突出亮点在于PBAP平台的模块化适配能力——相当于该平台是“可替换零件”的,能根据不同肿瘤调整,打破抗原限制。研究团队将病毒抗原替换为HER2蛋白结构域,构建了PBAP-HER2融合蛋白。在HER2阴性但PD-L1阳性的MDA-MB-231乳腺癌模型中,PBAP-HER2成功“标记”肿瘤细胞,使原本仅对HER2阳性肿瘤有效的曲妥珠单抗(Herceptin)及抗体药物偶联物Kadcyla(T-DM1)能够识别并杀伤HER2阴性肿瘤。
这一发现突破了抗体药物对抗原表达的绝对依赖,为临床上大量存在的抗原缺失型难治性肿瘤提供了超适应症治疗新思路,真正实现了一平台多靶点的通用型设计。
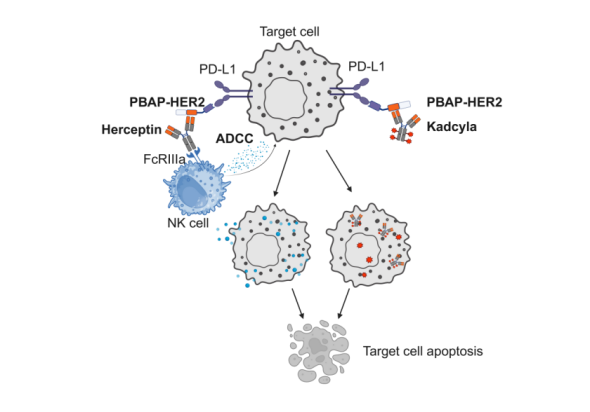
PBAP-Her2联合曲妥珠单抗(Herceptin)协同NK细胞或联合恩美曲妥珠单抗(Kadcyla, ADC)药物独立发挥抗肿瘤活性示意图
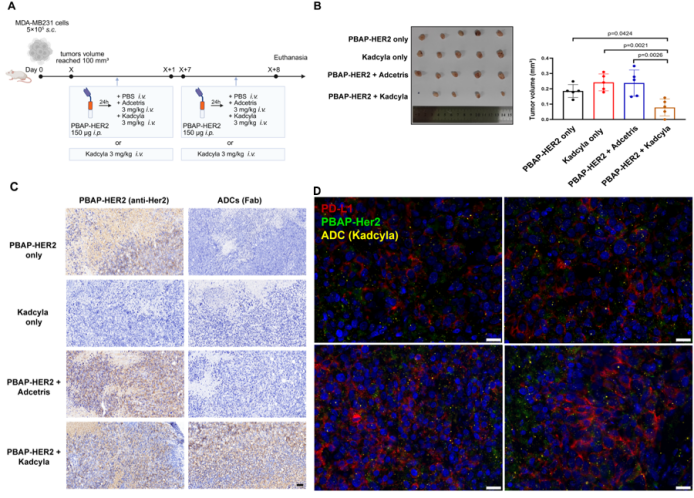
PBAP-HER2介导的抗原重定向使Kadcyla获得HER2阴性肿瘤(MDA-MB231)清除能力

临床优势:
低成本盘活既有免疫资源
相较于传统肿瘤免疫治疗手段,该“免疫桥接”策略展现出独特的临床经济学优势与转化潜力。它以即将上市的LZ901重组带状疱疹疫苗为核心依托,核心机制在于高效盘活接种者体内预存的抗gE抗体库——无需开发昂贵的肿瘤特异性单克隆抗体,仅需利用LZ901疫苗诱导的内源性免疫记忆作为桥接,即可低成本、高安全性地激活抗肿瘤免疫应答。
临床试验结果显示,LZ901疫苗在维持与葛兰素史克欣安立适(Shingrix)相当的保护效力的同时,展现出更高的安全性与更突出的细胞免疫优势。这种对预防性疫苗免疫资源的临床再应用,不仅规避了重复研发投入,还借助LZ901疫苗的性价比优势,极大提升了老年肿瘤患者的治疗可及性,实现了免疫资源的优化利用。
综上所述,该研究阐明了通过PBAP平台重定向预存疫苗免疫力的可行性,建立了连接抗病毒体液免疫与肿瘤细胞的“分子桥梁”。该研究填补了利用既有疫苗免疫力治疗肿瘤的策略空白,为开发下一代通用型肿瘤免疫治疗产品提供了理论基础与技术支撑。
邹帆为论文的通讯作者,广州妇女儿童医疗中心高惠昕、中山大学附属第三医院卢丽娟、深圳理工大学药学院熊晓晓和李一,以及湖北省第三人民医院胡东辉为论文的共同第一作者。该研究在深圳市基础研究专项自然科学基金计划面上项目、国家自然科学基金等经费的资助下完成。
该研究相关技术已经以深圳理工大学为专利权人申请了发明专利。
点击文末“阅读原文”查看论文
 来源:药学院责编:余彬审校:李韵、张吟越、王之康
来源:药学院责编:余彬审校:李韵、张吟越、王之康
为SUAT点个赞和在看吧

 高招云直播
高招云直播




